发布日期:2024-08-29 10:05 点击次数:90

左手螺旋核酸在结构上于右手螺旋核酸有很大不同。1970年,Robert D. Wells初次报说念了左手螺旋的双链DNA(Z-DNA)【1】。随后,Alexander Rich手脚最早商讨左手螺旋核酸的商讨者之一,他发现由胞嘧啶和鸟嘌呤形成的换取序列(CG-repeat DNA)大约在超高盐浓度下由右手螺旋缓助为左手螺旋并贯通出左手螺旋DNA的原子结构【2,3】。1981年,他利用溴化反映将溴分子插入CG-repeat DNA中,使其大约在生理盐浓度条款下寂静,进而用这种溴化的Z-DNA手脚抗原坐褥出特异性识别左手螺旋DNA的抗体【4】人妖 丝袜,为以后商讨左手螺旋核酸作念出进击孝敬。1984年,Thomas M. Jovin和Johan H. van de Sande发当今高盐浓度下RNA也不错呈现左手螺旋【5】。
跟着对左手螺旋核酸商讨的长远,一个问题随之而来,左手螺旋的核酸是否存在于当然界中。由于左手螺旋的DNA和RNA齐需要极高的盐浓度环境或荒谬的化学修饰能力在生理条款下保管寂静,商讨者一度认为它们不存在于当然界中,仅仅东说念主为的家具。然则在1987和1989年,Andrew H. Zarling以及Elissa P. Sena现实室通过哄骗特异识别Z-RNA的抗体进行免疫荧光染色,接踵在原核细胞和真核细胞上发现了Z-RNA存在的左证【6,7】。况且,大约识别并诱惑左手螺旋核酸的卵白质也接踵在各物种中被飘扬出来(如哺乳动物的ZBP1和ADAR1卵白)。记忆昔时40年的商讨,不错澄莹地得出一个论断,那就是左手螺旋核酸存在于当然界中,况且具有生物学功能。
好意思国Fox Chase癌症中心Siddharth Balachandran说明注解所指示的商讨团队一直神敢于商讨流感病毒(单链RNA病毒)所引起的宿主细胞物化机制。此前,该团队照旧飘扬出流感病毒在复制经过中会激活宿主细胞ZBP1-RIPK3-MLKL信号通路介导的细胞神气性坏死(Necroptosis)【8,9】。但是,流感病毒具体是如何激活这条信号通路仍不澄莹。
2020年3月19日,Siddharth Balachandran课题组(共统一手脚张霆和尹超然博士)在Cell上发表著作Influenza Virus Z-RNAs Induce ZBP1-Mediated Necroptosis,揭示了流感病毒是怎样一步一步指令宿主细胞序性坏死。

由于ZBP1是感应左手螺旋核酸的受体卵白,而流感病毒基因组是RNA,是否流感病毒大约产生Z-RNA从而激活ZBP1?作家需要护士的第一个问题即是如何检测Z-RNA。由于当本事离取得的识别Z-RNA的抗体齐莫得贸易化况且年代久远,导致如今已无法找到不错使用的识别Z-RNA的抗体。但是,1987年Charles C. Hardin就照旧讲解,由于Z-RNA和Z-DNA结构极为相似,一些识别Z-DNA的抗体相同大约识别Z-RNA【10】。因此,本文作家利用东说念主工合成的带标志的Z-RNA对现时悉数的贸易化识别Z-DNA抗体进行筛选,并得到了两个不错识别Z-RNA的抗体(图1)。通过免疫荧光染色和拔擢多样对照,作家说明了在被流感病毒感染的细胞核中有多半Z-RNA信号,况且当扼制病毒复制后Z-RNA信号会消失(图2)。ZBP1卵白主要漫步于细胞浆中,但当细胞被感染后,ZBP1卵白会赶快鼎新至细胞核并通过左手螺旋核酸识别域与Z-RNA诱惑。配体和受体的互相作用即Z-RNA与ZBP1诱惑,激励受体ZBP1活化并激活卑鄙RIPK3卵白。活化的RIPK3卵白进而激活MLKL(神气性细胞坏死的最终效应器)导致神气性坏死发生。
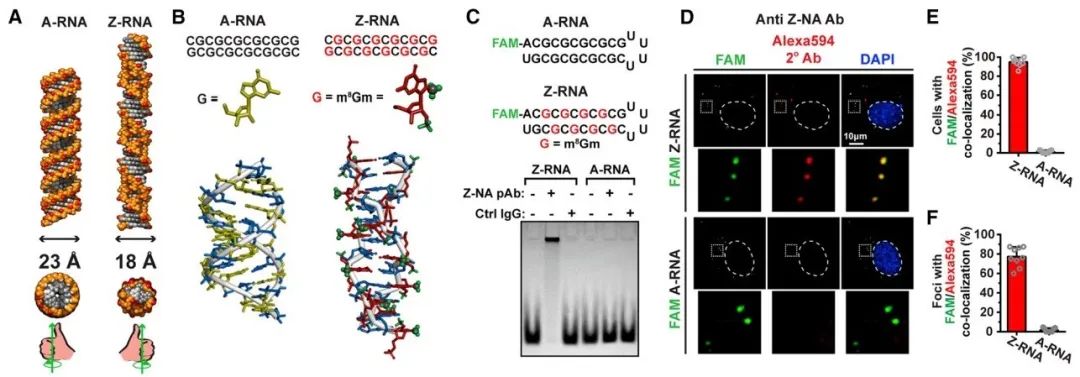
图1.筛选出识别Z-RNA的抗Z-DNA抗体。
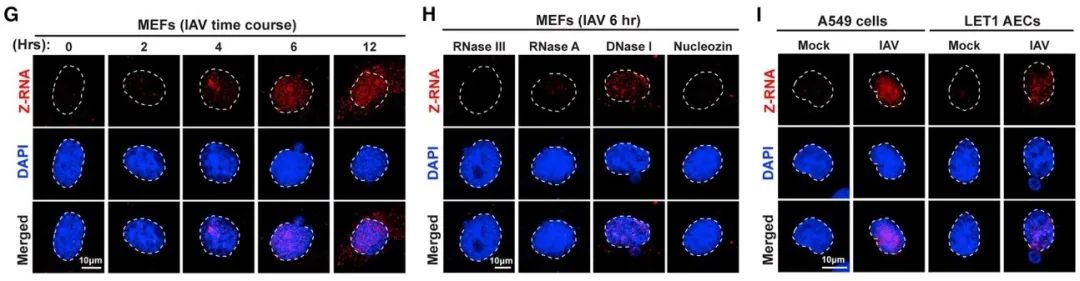
图2.流感病毒在宿主细胞核产生Z-RNA。
作家还发现,由于流感病毒是在宿主细胞核进行复制,ZBP1识别流感Z-RNA并最终激活MLKL的经过首先均发生于细胞核中。活化的MLKL不仅能报复细胞质膜也能报复核膜,并变成核膜不好意思满,染色质投入细胞浆。核膜的损害也会导致细胞在神气性坏死经过中开释更多的损害干系的分子口头(DAMPs)。通过体内现实,作家们进一步商讨发现,如若阻断神气性坏死(敲除mlkl基因),就不错灵验防碍嗜中性粒细胞在肺部的多半召募。嗜中性粒细胞的多半召募早已讲解是流感发病机制的主要元凶之一。
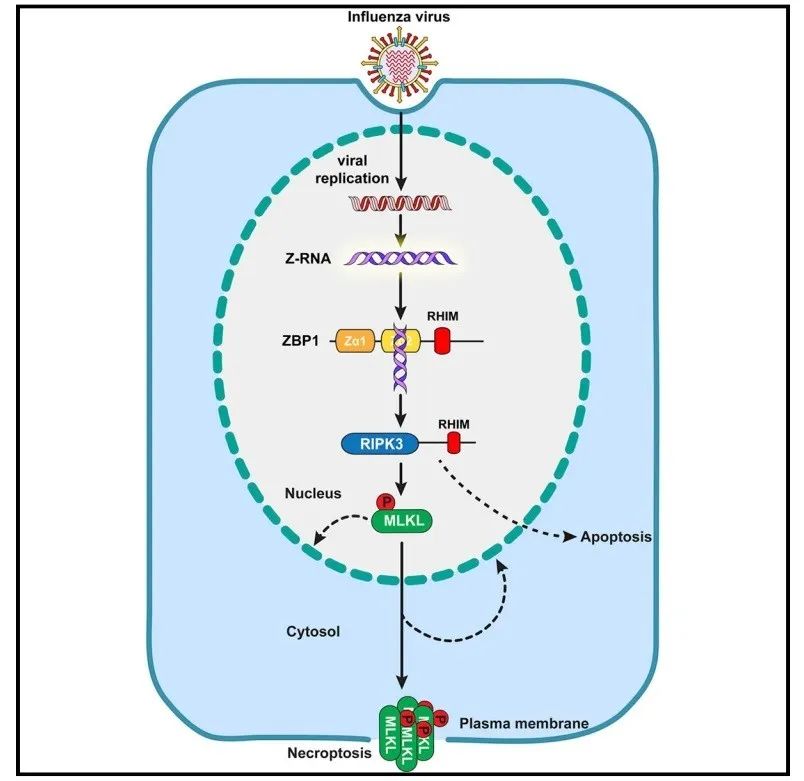
图3流感病毒激励宿主细胞神气性坏死机制。
本文通过一系列的实考据明了流感病毒在宿主细胞核复制经过中产生左手螺旋RNA(Z-RNA),这些Z-RNAs手脚配体激活受体ZBP1,进而触发由ZBP1端正的ZBP1-RIPK3-MLKL细胞神气性坏死信号通路(图3)。
原文标题:Influenza Virus Z-RNAs Induce ZBP1-Mediated Necroptosis
原文齐集:https://doi.org/10.1016/j.cell.2020.02.050
参考文件
1.Mitsui, Y., et al., Physical and enzymatic studies on poly d(I-C)-poly d(I-C), an unusual double-helical DNA. Nature, 1970. 228(5277): p. 1166-9.
2. Crawford, J.L., et al., The tetramer d(CpGpCpG) crystallizes as a left-handed double helix. Proc Natl Acad Sci U S A, 1980.77(7): p. 4016-20.
3. Wang, A.H., et al., Molecular structure of a left-handed double helical DNA fragment at atomic resolution. Nature, 1979.282(5740): p. 680-6.
4.Lafer, E.M., et al., Antibodies specific for left-handed Z-DNA. Proc Natl Acad Sci U S A, 1981. 78(6): p. 3546-50.
5.Hall, K., et al., 'Z-RNA'--a left-handed RNA double helix. Nature, 1984. 311(5986): p. 584-6.
6.Zarling, D.A., et al., Cytoplasmic Z-RNA. Proc Natl Acad Sci U S A, 1987. 84(17): p. 6117-21.
7.Zarling, D.A., et al., Cytoplasmic microinjection of immunoglobulin Gs recognizing RNA helices inhibits human cell growth. J Mol Biol, 1990. 211(1): p. 147-60.
8.Thapa, R.J., et al., DAI Senses Influenza A Virus Genomic RNA and Activates RIPK3-Dependent Cell Death. Cell Host Microbe, 2016. 20(5): p. 674-681.
9.Nogusa, S., et al., RIPK3 Activates Parallel Pathways of MLKL-Driven Necroptosis and FADD-Mediated Apoptosis to Protect against Influenza A Virus. Cell Host Microbe, 2016. 20(1): p. 13-24.
10.Hardin, C.C.人妖 丝袜, et al., Stabilization of Z-RNA by chemical bromination and its recognition by anti-Z-DNA antibodies.Biochemistry, 1987. 26(16): p. 5191-9.


